FcRnは主として細胞内に局在し、細胞内に取り込まれたIgG自己抗体を含むIgGとエンドソーム内(酸性条件下)で結合して、IgG自己抗体を含むIgGがリソソームに輸送されて分解されるのを抑制し、細胞外に再度放出(リサイクル)します。FcRnは、この機序によりIgG自己抗体を含むIgGの血中濃度を維持します1,2,3)。
ヒフデュラの作用機序
ヒフデュラの作用機序(動画)
【再生時間】 3分48秒
FcRn(胎児性FcRn受容体)は、IgG自己抗体を含むIgGの血中濃度を維持
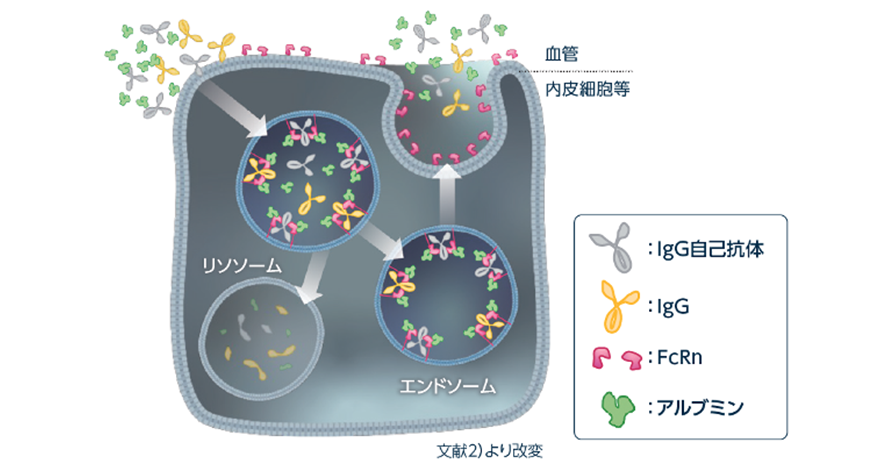
- FcRnとIgG自己抗体を含むIgGが結合する1)
- FcRnと結合したIgG自己抗体を含むIgGは、リソソームでの分解を免れる1)
- こうしてFcRnは、IgG自己抗体を含むIgGの循環(高い血中濃度)を維持する1)
1)Ulrichts P, et al.: J Clin Invest. 2018; 128(10): 4372-4386.本試験はargenx社の支援のもと行われた。著者に同社より研究助成金等を受領している者、同社の社員が含まれる。
2)Ward ES, et al.: Front Immunol. 2022; 13: 892534. 著者にargenx社の社員、同社より研究助成金等を受領している者が含まれる。https://creativecommons.org/licenses/by/4.0/
3)Anderson CL, et al.: Trends Immunol. 2006; 27(7): 343-348.
ヒフデュラは、エフガルチギモドにボルヒアルロニダーゼを配合した皮下投与用注射製剤
エフガルチギモドは、胎児性Fc受容体(FcRn)を標的とするアミノ酸残基を改変したヒトIgG1抗体のFcフラグメントです1)。

1)Howard JF Jr, et al.: Lancet Neurol. 2021; 20(7): 526-536.
ボルヒアルロニダーゼは、エフガルチギモドの体内への拡散、吸収を促進
ボルヒアルロニダーゼは主に皮下組織の成分であるヒアルロン酸を加水分解し、一過性かつ局所的に皮下組織の浸透性を増加させ1,2)、エフガルチギモドの体内への拡散、吸収を促進させます1,3)。
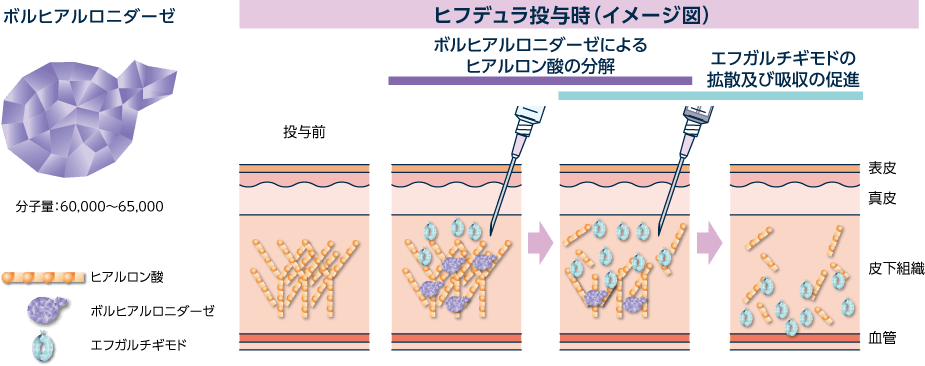
1) ヒフデュラ®配合皮下注 電子添文
2) Frost GI, et al.: Expert Opin Drug Deliv. 2007; 4(4): 427-440.
3) Locke KW, et al.: Drug Deliv. 2019; 26(1): 98-106.
エフガルチギモド: 血中アルブミン濃度を減少させず、 FcRnのIgGリサイクリングを標的とするFcフラグメント製剤1-3)
ヒフデュラ®には、胎児性Fc受容体(FcRn)を標的とするアミノ酸残基を改変したヒトIgG1抗体のFcフラグメント・エフガルチギモド4)が含まれています。
エフガルチギモドは内因性IgGのFcRnへの結合を競合阻害することによって、内因性IgGのリサイクルを阻害して、IgG分解を促進し、IgG自己抗体を含む血中IgG濃度を減少させます3,5)。
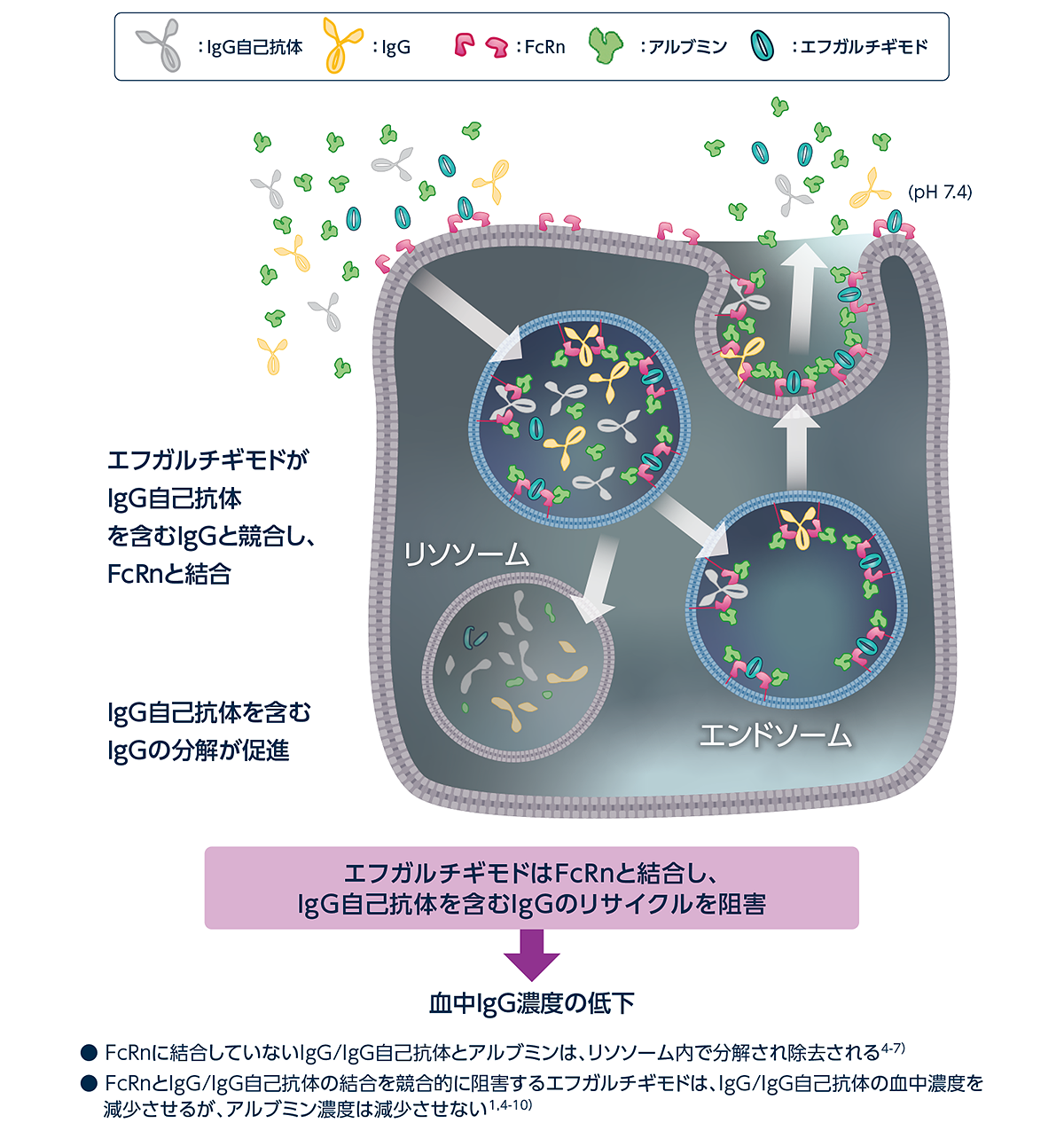
1)ウィフガート®点滴静注400mg 電子添文
2)Wolfe GI, et al.: J Neurol Sci. 2021; 430: 118074.(PMID:34563918)
[COI]著者にargenx社の社員、argenx社より研究助成金等を受領している者が含まれる。
3)Vaccaro C, et al.: Nat Biotechnol. 2005; 23(10): 1283-1288.(PMID:16186811)
4)Howard JF Jr, et al.: Front Neurol. 2024: 14: 1284444.(PMID:38318236)
[COI]本試験はargenx社の支援のもと行われた。著者に同社より研究助成金等を受領している者、同社の社員が含まれる。
5)Ulrichts P, et al.: J Clin Invest. 2018; 128(10): 4372-4386.(PMID:30040076)
[COI]本試験はargenx社の支援のもと行われた。著者に同社より研究助成金等を受領している者、同社の社員が含まれる。
6)Roopenian DC, Akilesh S. Nat Rev Immunol. 2007; 7(9): 715-725.(PMID:17703228)
7)Ward ES, Ober RJ. Trends Pharmacol Sci. 2018; 39(10): 892-904.(PMID:30143244)
[COI]著者にargenx社より研究助成金等を受領している者が含まれる。
8)Howard JF Jr, et al.: Lancet Neurol. 2021; 20(7): 526-536.(PMID:34146511)
[COI]本試験はargenx社の支援のもと行われた。著者に同社より研究助成金等を受領している者、同社の社員が含まれる。
9)Howard JF Jr, et al.: Neurology. 2019; 92(23): e2661-e2673.(PMID:31118245)
[COI]本試験はargenx社の支援のもと行われた。著者にargenx社の社員、同社より研究助成金等を受領している者が含まれる。
10)Ma G, et al.: JCI Insight. 2024; 9(10): e176166.(PMID:38713534)
[COI]著者にargenx社の社員、同社より研究助成金等を受領している者が含まれる。
エフガルチギモドは生理的な内因性IgGと同様に、Fc領域にFcRnとの結合部位を有し、ヒトIgG1に近い細胞内挙動を示した(in vitro)
FcRnは、MHCクラスI分子に類似した構造を持ち、α鎖とβ鎖(β2m※)の2つのポリペプチド鎖からなるヘテロ二量体を形成する受容体です。
生理的な内因性IgGは、Fc領域でFcRnと、中性下では結合せず、酸性下で結合します。
生体内IgG
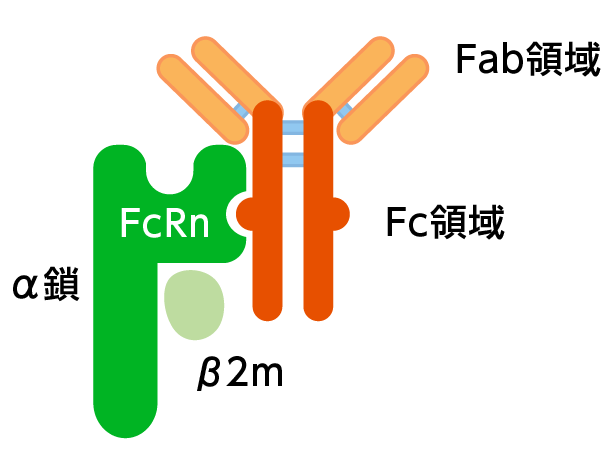
フラグメント製剤であるエフガルチギモドは、Fc領域でFcRnと、中性下(結合親和性:8.59±1.35)と酸性下(結合親和性:0.35±0.06)の両方で結合します※。
※社内資料:カニクイザル内因性IgGに対する薬理作用(承認時評価資料)(CTD2.6.2.2.3.2.3)
IgG1‐Fcフラグメント

その他に、構造によって以下のような結合様式があることが報告されています。
その他
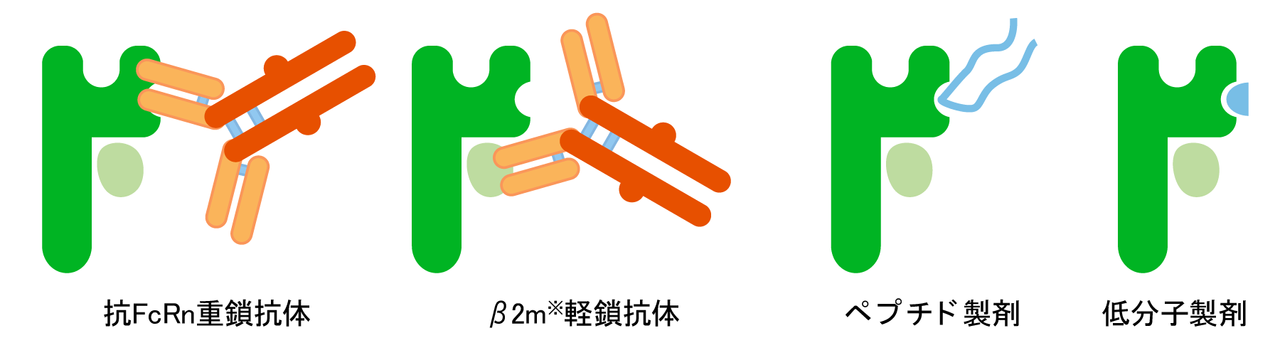
※ β2m; β2ミクログロブリン
1)Sockolosky & Szoka, Adv Drug Deliv Rev. 2015 Aug 30;91:109-24.より改変
In vitroにおいて、エフガルチギモドはヒトIgG1に近い細胞内輸送挙動を示しました。
エフガルチギモド、ヒトIgG1及び完全長抗FcRn抗体の細胞内挙動(in vitro)2)
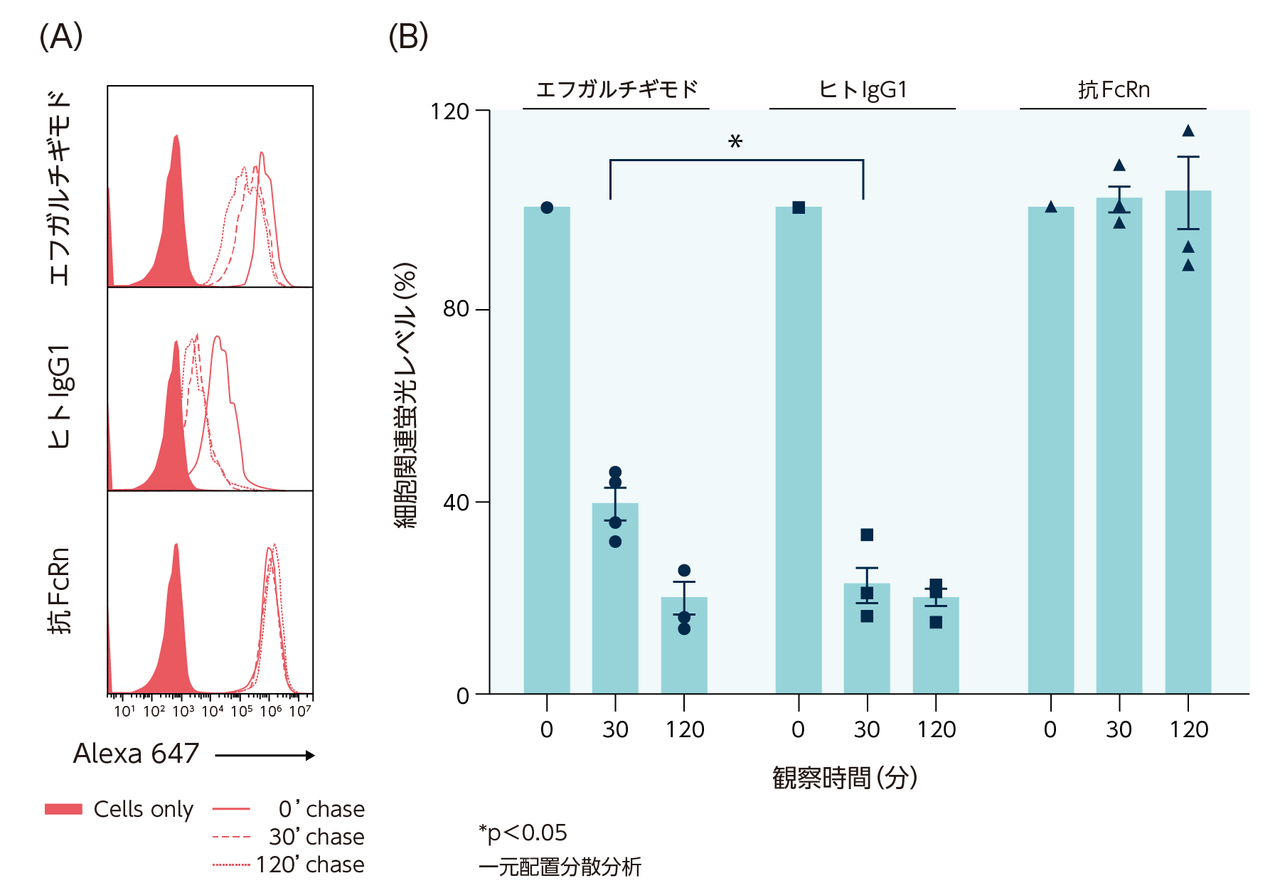
試験方法:hFcRn-GFP(緑色蛍光タンパク質)を発現する内皮細胞(HMEC-1)に、蛍光標識したエフガルチギモド、ヒトIgG1(アイソタイプコントロール)、完全長抗FcRn抗体(完全ヒトモノクローナル抗体)をそれぞれ25、200、及び75μg/mLでパルスし、0、30及び120分間観察した。
2)Ulrichts P, et al.: J Clin Invest. 2018; 128(10): 4372-4386
[COI] 本試験はargenx社の支援のもと行われた。著者にargenx社よりコンサルタント料等を受領している者が含まれる。
また、著者にargenx社の社員が含まれる。
エフガルチギモドの投与により、IgG以外の免疫グロブリン濃度への影響はなく、アルブミン濃度の減少は認められていない
健康成人に、エフガルチギモドを1週間間隔で4回2時間かけて静脈内投与したときのIgA、IgD、IgE、IgM、アルブミンの血清濃度(%T0)のベースラインに対する変化率は下図の通りでした。
IgA、IgD、IgE、IgM、及びアルブミンの血中濃度に及ぼす影響(健康成人)
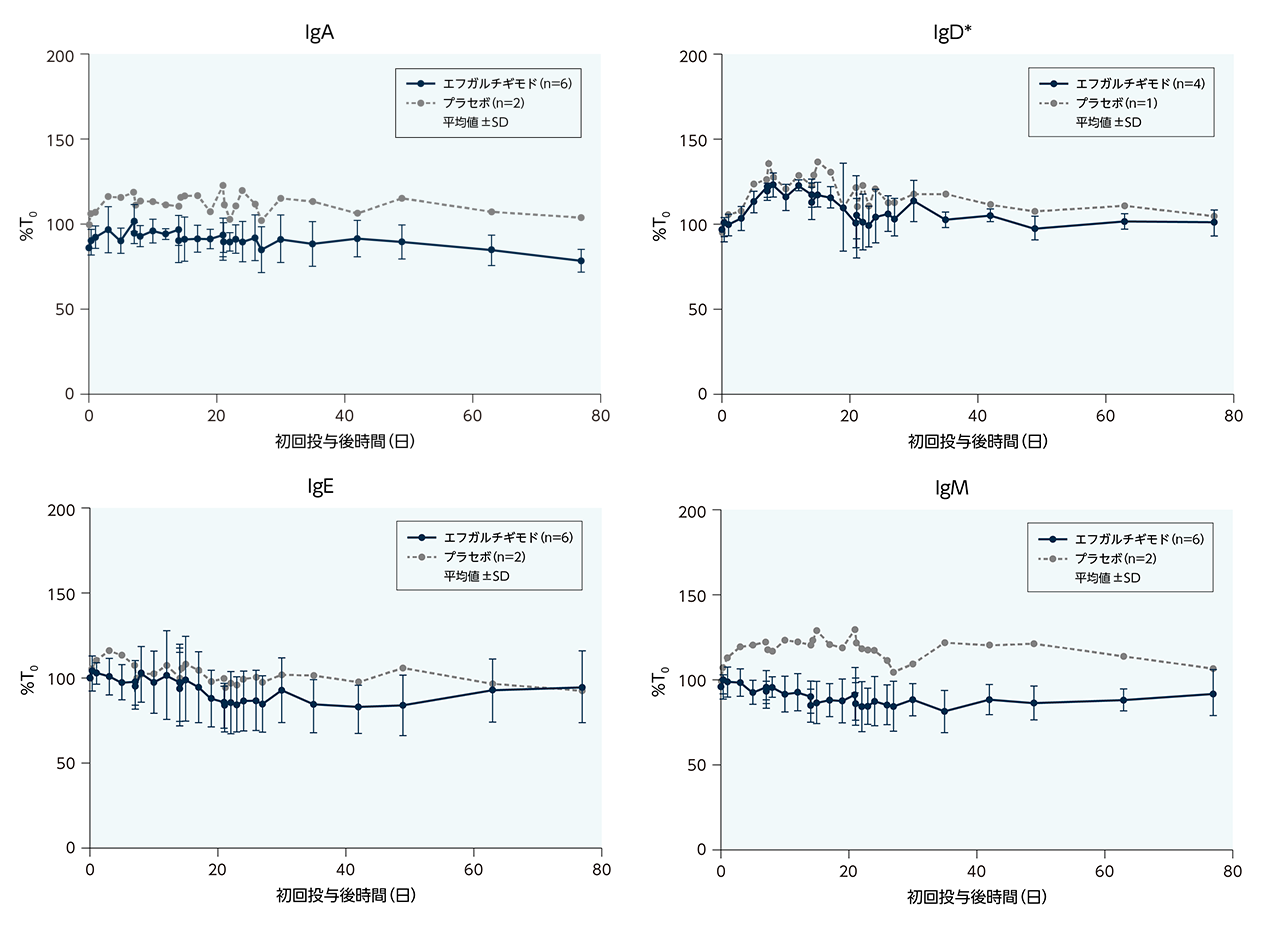
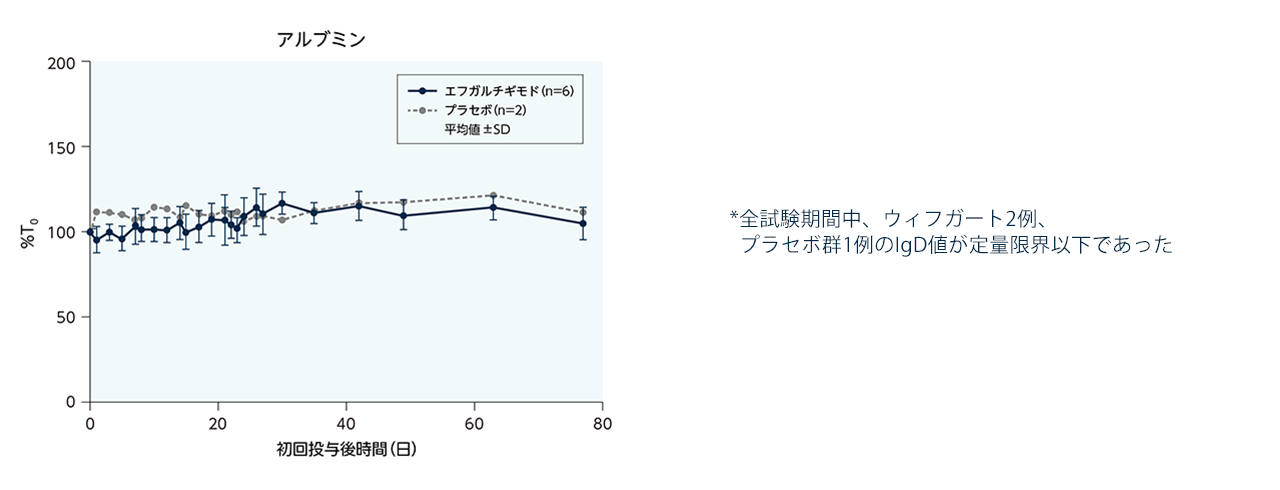
試験方法:健康成人(n=8)に、25mg/kgのエフガルチギモドまたはプラセボ(6:2でランダム化)を1週間間隔で4回2時間かけて静脈内投与した。IgA、IgD、IgE、IgM、アルブミンの血清濃度(%T0)のベースラインに対する変化率を示す。
※本邦で承認されたヒフデュラの用法及び用量:
〈慢性炎症性脱髄性多発根神経炎〉
【ヒフデュラ®配合皮下注】通常、成人には本剤1回5.6mL(エフガルチギモド アルファ(遺伝子組換え)として1,008mg及びボルヒアルロニダーゼ アルファ(遺伝子組換え)として11,200単位)を週1回皮下投与する。
【ヒフデュラ®配合皮下注シリンジ】通常、成人には本剤1回5.0mL(エフガルチギモド アルファ(遺伝子組換え)として1,000mg及びボルヒアルロニダーゼ アルファ(遺伝子組換え)として10,000単位)を週1回皮下投与する。
2)Ulrichts P, et al.: J Clin Invest. 2018; 128(10): 4372-4386
[COI] 本試験はargenx社の支援のもと行われた。著者にargenx社よりコンサルタント料等を受領している者が含まれる。
また、著者にargenx社の社員が含まれる。
おすすめコンテンツ
JP-VDJCIDP-25-00752(2025年12月作成)
